Elektrode: Anode Vs. Kathode - Was Du Wissen Musst!
Verwirrt über die Welt der Elektrizität und Chemie? Es ist entscheidend, die Polarität einer Elektrode zu verstehen, um die Funktionsweise von Batterien, Elektrolyse und anderen elektrochemischen Prozessen zu begreifen. Die positive Elektrode, oft auch Kathode genannt, spielt dabei eine zentrale Rolle.
Die Elektrode, ein Begriff, der vom griechischen Wort "elektron" (Bernstein) abgeleitet ist, ist ein elektrischer Leiter, der verwendet wird, um Kontakt mit einem nichtmetallischen Teil eines Stromkreises herzustellen, beispielsweise einem Elektrolyten. Innerhalb dieses Rahmens ist die positive Elektrode ein Schlüsselakteur, besonders in elektrochemischen Zellen und Geräten. Sie ist der Pol, zu dem die Elektronen fließen und an dem die Reduktion stattfindet – der Prozess der Elektronenaufnahme. Um die Bedeutung der positiven Elektrode vollständig zu erfassen, ist es unerlässlich, ihre Eigenschaften, ihre Funktion in verschiedenen Anwendungen und ihr Verhältnis zu anderen Komponenten wie der Anode zu untersuchen. Tauchen wir tiefer in die Welt der positiven Elektrode ein, um ihre komplexen Mechanismen und ihre Bedeutung in unserem technologischen Alltag zu verstehen.
| Aspekt | Details zur positiven Elektrode (Kathode) |
|---|---|
| Definition | Elektrode, zu der Elektronen fließen; Ort der Reduktion (Elektronenaufnahme). |
| Polarität | Positives Potenzial relativ zur Anode (in galvanischen Zellen).Je nach Anwendung (Elektrolysezellen) positiv oder negativ. |
| Funktion in Batterien | Akzeptiert Elektronen, die von der Anode freigesetzt werden, wodurch ein Stromkreis entsteht.Bestimmt zusammen mit dem Anodenmaterial die Spannung und Kapazität der Batterie. |
| Materialien | Lithium-Metalloxide (LiCoO2, LiMn2O4, LiFePO4), Nickel-Metallhydroxide (Ni(OH)2), Mangandioxid (MnO2), Blei(IV)-oxid (PbO2) u.v.m. |
| Funktion in der Elektrolyse | Elektrode, an der die Oxidation von Anionen stattfindet.Bsp.: Bei der Elektrolyse von Wasser entsteht Sauerstoff an der Anode. |
| Funktion beim Eloxieren | Die Anode (das zu eloxierende Metall) wird zur positiven Elektrode. |
| Beziehung zur Anode | Die Anode ist die Elektrode, an der die Oxidation stattfindet (Elektronen werden freigesetzt).Kathode und Anode bilden zusammen eine elektrochemische Zelle. |
| Historischer Kontext | Der Begriff "Kathode" wurde von William Whewell geprägt und leitet sich von den griechischen Wörtern "kato" (abwärts) und "hodos" (Weg) ab. |
| Wichtige Überlegungen | Materialauswahl beeinflusst Leistung, Kosten und Umweltverträglichkeit.Die Stabilität und Leitfähigkeit der positiven Elektrode sind entscheidend für die Lebensdauer des Geräts. |
| Anwendungen | Batterien (Lithium-Ionen, Blei-Säure, Nickel-Metallhydrid), Brennstoffzellen, Elektrolyse, Eloxieren, Sensoren. |
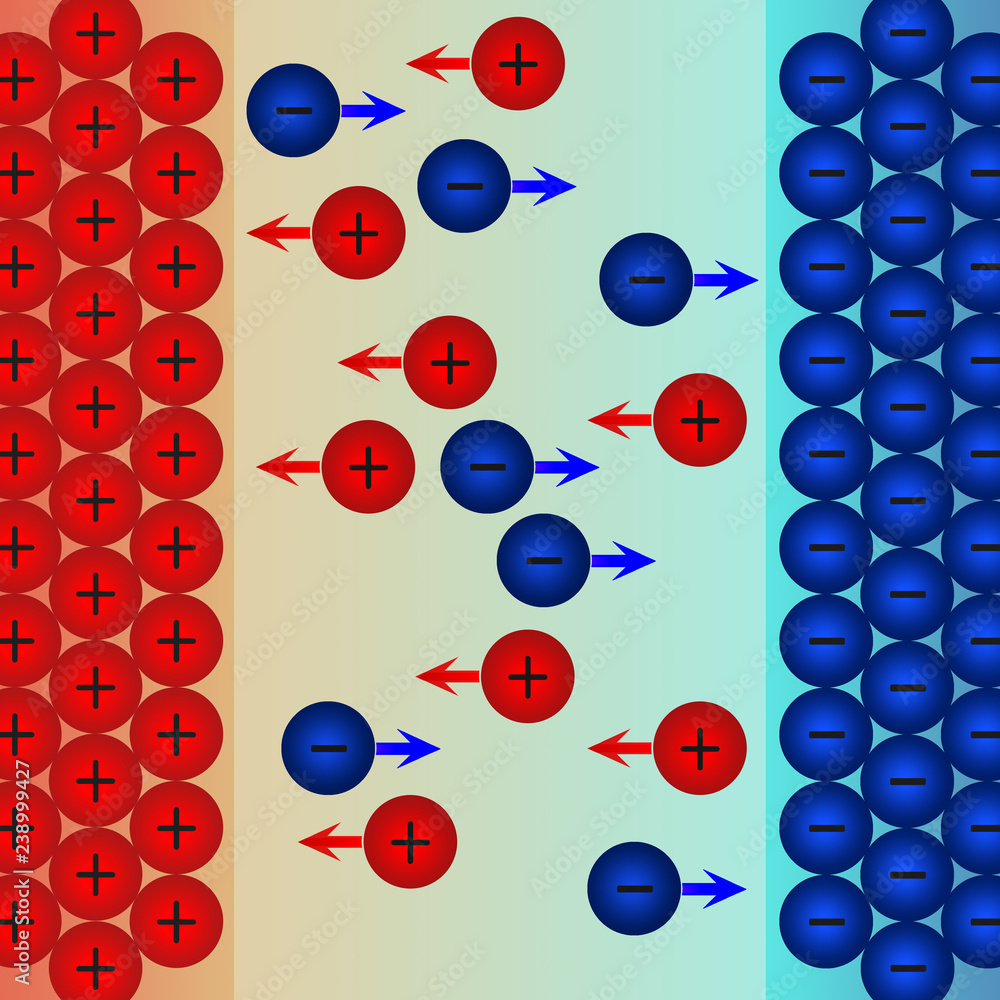
Die positive Elektrode, oft auch Kathode genannt, ist in vielerlei Hinsicht das Gegenstück zur Anode. Um die Verwirrung zu vermeiden, ist es wichtig, die Unterschiede klar zu definieren. In einer Batterie ist die Kathode die positive Elektrode, während die Anode die negative Elektrode ist. Die Elektronen fließen von der Anode zur Kathode, was den Stromfluss im externen Kreislauf ermöglicht. Die Reduktion, also die Aufnahme von Elektronen, findet an der Kathode statt, während die Oxidation, also die Abgabe von Elektronen, an der Anode stattfindet.
- Gelbe Blumen Im Garten Bedeutung Auswahl Tipps
- Arteria Subclavia Anatomie Funktion Erkrankungen Alles Wichtige
Der Name "Kathode" wurde von William Whewell geprägt und leitet sich von den griechischen Wörtern κάτω (kato), 'abwärts', und ὁδός (hodós), 'ein Weg', ab. Diese Namensgebung spiegelt die Richtung des Stromflusses wider, der traditionell als die Bewegung positiver Ladungsträger definiert wurde. Die Elektrode ist also der "Weg abwärts" für den (positiven) Strom.
Die Frage, ob die Anode positiv oder negativ ist, hängt vom jeweiligen elektrochemischen System ab. In einer galvanischen Zelle (z.B. einer Batterie) ist die Anode negativ, da sie die Quelle der Elektronen ist. In einer Elektrolysezelle hingegen ist die Anode positiv, da sie an eine positive Spannungsquelle angeschlossen ist, die die Elektronen aus dem Elektrolyten zieht.
Die positive Elektrode spielt eine entscheidende Rolle in verschiedenen Anwendungen. In Lithium-Ionen-Batterien, die heutzutage weit verbreitet sind, besteht die positive Elektrode üblicherweise aus einem Lithium-Metalloxid wie Lithiumcobaltoxid (LiCoO2), Lithiumnickeloxid (LiNiO2) oder Lithiummanganoxid (LiMn2O4). Diese Materialien ermöglichen die reversible Insertion und Extraktion von Lithiumionen, was den Lade- und Entladevorgang der Batterie ermöglicht.
- Radsetzerei Berlin Veranstaltungen Tim Burtons Labyrinth Jetzt Tickets
- Entdecke Jetzt Clube Porto Mos Dein Algarvetraumurlaub Wartet
Die Leistung einer Lithium-Ionen-Batterie hängt stark von den Eigenschaften des Materials der positiven Elektrode ab. Faktoren wie die spezifische Kapazität, die Spannungsstabilität und die Ionenleitfähigkeit spielen eine entscheidende Rolle. Die Forschung konzentriert sich daher auf die Entwicklung neuer Materialien für positive Elektroden, die eine höhere Energiedichte, eine längere Lebensdauer und eine verbesserte Sicherheit bieten.
Neben Lithium-Ionen-Batterien finden positive Elektroden auch in anderen Batterietypen Verwendung, wie z.B. Blei-Säure-Batterien (Blei(IV)-oxid an der positiven Elektrode) und Nickel-Metallhydrid-Batterien (Nickel(II)-hydroxid an der positiven Elektrode). Auch in Brennstoffzellen spielt die positive Elektrode eine wichtige Rolle bei der Katalyse der elektrochemischen Reaktionen.
Die Elektrolyse ist ein weiterer wichtiger Anwendungsbereich für positive Elektroden. Bei der Elektrolyse wird eine elektrische Spannung angelegt, um eine chemische Reaktion zu erzwingen. Beispielsweise kann Wasser durch Elektrolyse in Wasserstoff und Sauerstoff zerlegt werden. Die Sauerstoffentwicklung findet dabei an der positiven Elektrode (Anode) statt, während die Wasserstoffentwicklung an der negativen Elektrode (Kathode) stattfindet.
Ein weiteres Beispiel ist die Eloxierung von Aluminium. Beim Eloxieren wird eine Schutzschicht aus Aluminiumoxid auf der Oberfläche des Aluminiums erzeugt. Das Aluminiumbauteil dient dabei als Anode (positive Elektrode) in einem Elektrolyten, typischerweise Schwefelsäure. Durch die Elektrolyse bildet sich eine Oxidschicht auf der Oberfläche des Aluminiums, die es korrosionsbeständiger und verschleißfester macht.
Der Separator in einer Batterie oder einer elektrochemischen Zelle verhindert den direkten Kontakt zwischen der positiven und der negativen Elektrode, was zu einem Kurzschluss führen würde. Der Separator ist ein poröses Material, das den Transport von Ionen zwischen den Elektroden ermöglicht, aber den Durchgang von Elektronen verhindert.
Beim Entladen einer Batterie fließen die Elektronen vom unedleren Metall (negative Elektrode/Anode) zum edleren Metall (positive Elektrode/Kathode). Dieser Elektronenfluss erzeugt den elektrischen Strom, der zum Betrieb von Geräten verwendet werden kann.
In traditionellen Lithium/Natrium-Batterien ist die positive Elektrode üblicherweise eine Verbindung, die Lithium/Natrium-Ionen enthält, wie z.B. Schichtoxide, Spinelloxide und Phosphate. Die Elektrolyt-Ionen werden aus der positiven Elektrode extrahiert und sind an der Kationen-Doppelschichtbildung mit der kohlenstoffhaltigen Elektrode beteiligt, um die Ladungsneutralität in der Zelle aufrechtzuerhalten.
Dies gilt insbesondere für das letzte Jahrzehnt. In der Anfangszeit dominierten kohlenstoffhaltige Materialien die negative Elektrode, und daher wurden die meisten der möglichen Verbesserungen in der Zelle am positiven Anschluss erwartet.
Die Eloxierung ist ein elektrochemischer Prozess. Beim Eloxieren dient das Metall (Anode) als positive Elektrode, während eine Kathode (meist aus Blei oder Edelstahl) an den Minuspol der Stromversorgung angeschlossen wird. Der Elektrolyt, typischerweise Schwefelsäure, fungiert als Medium für die elektrochemische Reaktion.
Die Elektrolyse ist immer nach dem gleichen Prinzip aufgebaut. Wir brauchen eine positive Elektrode (Anode), eine negative Elektrode (Kathode) und eine Flüssigkeit (Elektrolyt), die die Elektroden umgibt und in der sich geladene Teilchen (Ionen) frei bewegen können.
In diese Elektrode fließt Strom:
Von dieser Elektrode fließt der Strom ab:
Die Anode hat normalerweise ein positives Potential (d.h. im Vergleich zur Kathode), die Kathode hat normalerweise ein negatives Potential (negative Elektrode) verhält sich in der Regel wie ein Elektronenträger:
Verhält sich in der Regel wie ein Elektronenakzeptor.
Es ist wichtig zu beachten, dass sich die Bezugsrichtung für den Stromfluss auf positive Ladungsträger bezieht und damit der Bewegungsrichtung von Elektronen entgegengesetzt ist. Daher fließt der Strom in einem Stromkreis von der positiven Elektrode (Kathode) zur negativen Elektrode (Anode), obwohl sich die Elektronen in die entgegengesetzte Richtung bewegen.
Weitere Materialien für die positive Elektrode sind beispielsweise Lithiumcobaltoxid (LiCoO2), Lithiumnickeloxid (LiNiO2) oder der Spinell Lithiummanganoxid (LiMn2O4).
Heutzutage wird Aluminium immer noch mit der Schmelzflusselektrolyse gewonnen.
Eine Elektrode [elɛkˈtroːdə] (von altgriechisch ἤλεκτρον elektron, „Bernstein“, i.e. wegen der elektrostatischen Aufladung durch Reibung) ist ein elektrischer Leiter, der Kontakt zu einem Medium herstellt, das nichtmetallisch ist und in dem ein Ionen- oder Elektronenfluss stattfindet. Dieses Medium kann ein Elektrolyt, ein Vakuum oder ein Halbleiter sein.
Ein Lithium-Ionen-Akku folgt dem Aufbau der galvanischen Zelle. Er besteht aus einer negativen Elektrode aus Graphit.
![Kathode • einfach erklärt Definition, Elektrolyse · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2021/03/WordPress_Bilder_Kathode_1-1-1024x576.png)
![Kathode • einfach erklärt Definition, Elektrolyse · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2021/03/WordPress_Bilder_Kathode_2-1-1024x576.png)
Detail Author:
- Name : Viva Effertz
- Username : ohermann
- Email : gianni.schmidt@mclaughlin.com
- Birthdate : 1987-10-11
- Address : 32406 Armand Fort Lake Cleo, WI 01147
- Phone : 928-421-6735
- Company : Mayer-Sawayn
- Job : Marine Engineer
- Bio : Sunt mollitia sit repudiandae corrupti qui doloribus at. Facilis possimus aut explicabo nostrum adipisci. Dolor neque commodi quos.
Socials
tiktok:
- url : https://tiktok.com/@yazmin_official
- username : yazmin_official
- bio : Unde ea soluta necessitatibus est.
- followers : 3436
- following : 1375
twitter:
- url : https://twitter.com/yazmin_abernathy
- username : yazmin_abernathy
- bio : Quibusdam deleniti exercitationem architecto sed. Voluptas eos ut facere officia velit nulla. Doloremque enim totam vero adipisci.
- followers : 776
- following : 316